摘要:3月27日,港股科技創新型醫藥企業遠大醫藥(0512.HK)再度傳來利好,公司與聯拓生物科技有限公司(下稱:聯拓生物)和TarsusPharmaceuticals,Inc.(下稱:Tarsus)達成產品引進戰略合作協議。
3月27日,港股科技創新型醫藥企業遠大醫藥(0512.HK)再度傳來利好,公司與聯拓生物科技有限公司(下稱:聯拓生物)和Tarsus Pharmaceuticals, Inc.(下稱:Tarsus)達成產品引進戰略合作協議。相關條件滿足后,遠大醫藥將以1,500萬美元的首付款及一定金額的注冊里程碑費用取得用于治療蠕形螨瞼緣炎及蠕形螨導致的瞼板腺功能障礙的全球創新眼用制劑TP-03在大中華區(中國大陸、中國香港、中國澳門、中國臺灣)的獨家開發、生產及商業化權益。
據悉,TP-03已于2023年7月獲得美國FDA批準上市,是目前FDA批準的首款也是唯一一款針對蠕形螨瞼緣炎的藥物。我國尚未有針對蠕形螨瞼緣炎的藥物上市,此次交易完成后,遠大醫藥將大力推進TP-03在中國的注冊落地工作,盡早惠及國內廣大蠕形螨瞼緣炎患者,同時也將深化公司在五官科領域的產品布局。
TP-03臨床數據優勢顯著,為FDA唯一獲批蠕形螨瞼緣炎藥物
根據公告,是一款對γ-氨基丁酸門控氯離子通道(GABA-Cl)具有選擇性的非競爭性拮抗劑,其通過選擇性抑制蠕形螨體內的GABA-Cl,使蟲體麻痹和死亡,進而徹底治愈蠕形螨瞼緣炎。此外,TP-03具有高度親脂性,可促進其在螨蟲棲息的睫毛毛囊油脂中的吸收。
臨床試驗方面,TP-03已在美國完成了兩項關鍵性臨床研究,共入組800余名蠕形螨瞼緣炎患者,根據臨床結果顯示,兩項研究均達到了主要終點和所有次要終點,具有統計學意義,且未發生與治療相關的嚴重不良事件。該產品已于二零二三年七月獲得美國FDA批準上市,是目前FDA批準的首款也是唯一一款針對蠕形螨瞼緣炎的藥物。此外,TP-03在美國開展的用于治療蠕形螨導致的瞼板腺功能障礙的II期臨床研究也顯示出了陽性的頂線結果。
中國的Ⅲ期臨床結果顯示,與對照組相比,TP-03治療蠕形螨瞼緣炎患者的蠕形螨感染根除率具有統計學顯著性(p<0.001),眼瞼袖套狀分泌物治愈率也呈現出陽性但無統計學意義的趨勢(p=0.15)。此外,TP-03耐受性良好,其安全性特征與其他大規模臨床試驗中觀察到的結果相似,無治療相關的停藥情況。
TP-03或填補國內市場空白,惠及千萬蠕形螨瞼緣炎患者
據悉,瞼緣炎是一種常見的眼科疾病。蠕形螨瞼緣炎是蠕形螨感染瞼緣所致的慢性炎性反應性疾病,約占所有瞼緣炎病例的三分之二以上,主要累及瞼緣皮膚、睫毛囊和腺體以及瞼板腺,臨床表現主要為眼氧、眼異物感、眼干、瞼緣充血、鱗屑及睫毛根部袖套狀分泌物等,嚴重者可引起結膜及角膜并發癥,對瞼緣的破壞較大,容易復發且具備一定傳染性。
蠕形螨也是瞼板腺功能障礙的危險因素之一,蠕形螨導致的瞼板腺功能障礙患者常出現眼瞼邊緣發炎和視力模糊,并可能導致瞼板腺堵塞和/或瞼脂液分泌的減少,若不及時接受治療,可能會導致淚膜永久性改變和進行性腺體喪失。
根據弗若斯特沙利文數據,2021年全球蠕形螨瞼緣炎的患者人數已有約4.68億人;預計到2030年全球患者將達約5.06億人,其中中國患者約5,980萬人。數據顯示,美國蠕形螨性瞼緣炎影響著約2,500萬眼部護理患者,即每12名成人中就有1名蠕形螨性瞼緣炎患者。中國患者規模是美國患者的1倍多,同時,我國還有近7,000萬瞼板腺功能障礙患者,相應臨床需求十分可觀。
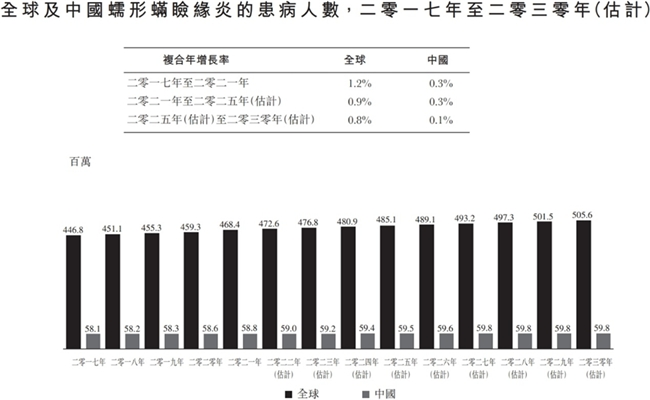
(數據來源:弗若斯特沙利文)
我國目前并沒有針對蠕形螨瞼緣炎的藥物上市,臨床治療蠕形螨主要以局部除螨為主,常用的藥物有茶樹油制劑、甲硝唑凝膠,但由于用藥周期較長且用藥后病灶局部的有效藥物濃度難以保證,導致治療效果有限,且其中甲硝唑功效相關數據有限,目前FDA并未批準其用于蠕形螨瞼緣炎。而新興治療手段如強脈沖光療法可能影響角膜上皮損傷修復,其安全性還有待觀察。因此,臨床上急需一款起效快且可直接作用于病灶深部的安全有效的治療藥物,而遠大醫藥此次布局的TP-03則有望填補這部分臨床空白,為蠕形螨瞼緣炎患者帶來新的治療選擇。
創新布局夯實五官科領軍地位,驅動業務領域新突破
值得注意的是,遠大醫藥作為中國主要的五官科藥物研發、生產及銷售綜合企業之一,公司在售產品管線數量位居行業前列,治療領域覆蓋眼科、耳鼻喉科、口腔科等多科室疾病,其產品覆蓋了化學制劑、中藥制劑及健康產品,包含處方藥、OTC、器械、消費品等幾大類別。經過多年的深耕,公司已實現了院內院外全渠道覆蓋,并持續打造集“預防+治療+保健”為一體的“大五官生態圈”。
創新研發方面,公司儲備了治療“近視”、“干眼癥”、“翼狀胬肉”和“眼科術后抗炎鎮痛”的多款全球創新產品,且在2023年內均取得了重大研發進展。其中,治療翼狀胬肉的創新產品CBT-001于2023年3月獲批在中國開展III期臨床研究;治療干眼癥的小分子多肽藥物GPN00136 (BRM421)于2023年4月獲批在中國開展II期臨床研究;用于抗炎鎮痛的激素納米混懸滴眼液GPN00833于2023年10月完成中國III期臨床試驗的首例患者入組給藥,并于2024年3月獲得美國FDA批準上市;用于推遲兒童近視進展的全球創新眼科藥物GPN00884于2024年3月獲批在中國開展I期臨床研究。

(圖片來源:遠大醫藥微信公眾號)
憑借著豐富的產品管線及差異化的創新產品布局,遠大醫藥已在五官科領域積累了雄厚的競爭優勢。對于未來發展,遠大醫藥表示,公司將秉持中西聯合和藥械同治的發展戰略,不斷強化行業影響力,實現業務領域新突破,并為全球患者提供更先進更多樣的治療方案。
8月19日,港股科技創新型醫藥企業遠大醫藥(00512.HK)中期業績報喜,公司上半年實現收入約60...
 2024-08-20
2024-08-208月17日,港股科技創新型醫藥企業遠大醫藥(0512.HK)發布公告稱,公司主研發的用于治療膿毒癥的...
 2023-08-17
2023-08-17近日,遠大醫藥(0512.HK)在放射性核素偶聯藥物(RDC)領域的重要戰略合作伙伴Telix Ph...
 2023-06-19
2023-06-19投資家網(www.51baobao.cn)是國內領先的資本與產業創新綜合服務平臺。為活躍于中國市場的VC/PE、上市公司、創業企業、地方政府等提供專業的第三方信息服務,包括行業媒體、智庫服務、會議服務及生態服務。長按右側二維碼添加"投資哥"可與小編深入交流,并可加入微信群參與官方活動,趕快行動吧。
